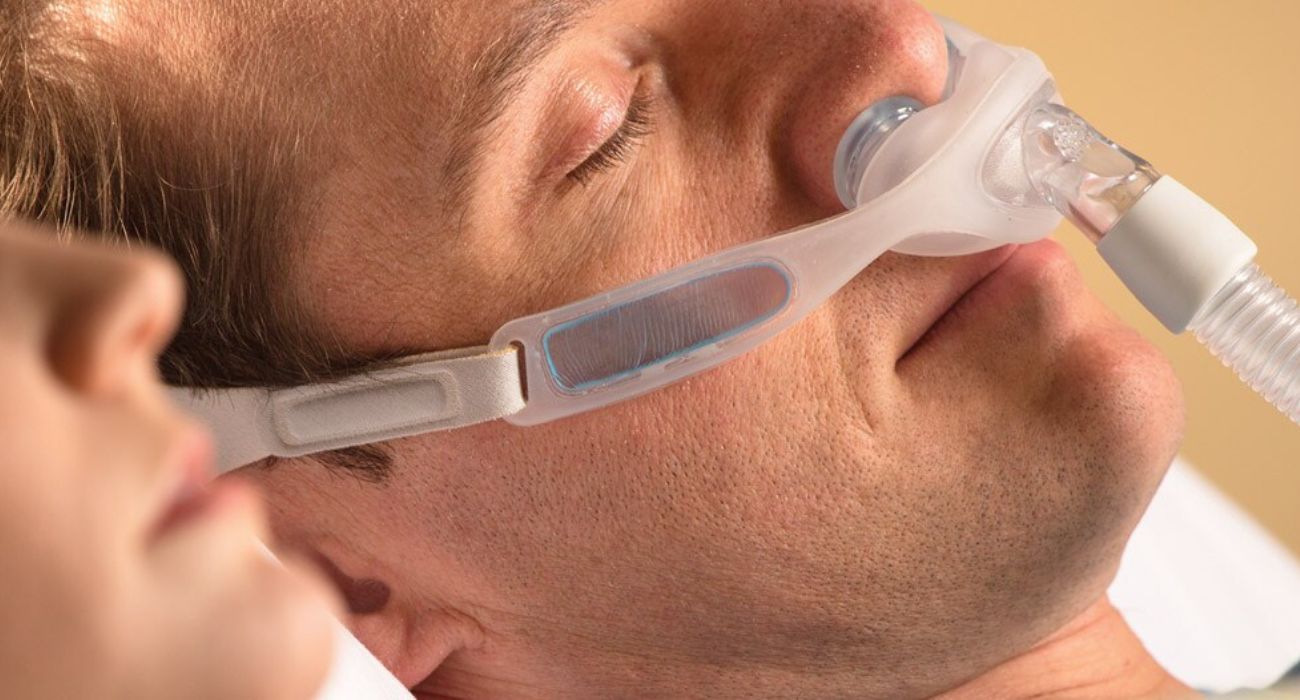
La empresa de tecnología sanitaria Philips está deteniendo las ventas de sus dispositivos para la apnea del sueño en Estados Unidos tras preocupaciones de seguridad y cientos de muertes relacionadas.
La Administración de Alimentos y Medicamentos inicialmente anunció en 2021, se retiraron del mercado varias máquinas BiPAP y CPAP, así como ventiladores fabricados por Philips Respironics, debido a preocupaciones sobre la descomposición de la espuma de poliuretano a base de poliéster en los dispositivos.
“Si esto ocurre, la persona que utiliza el dispositivo podría inhalar o tragar trozos negros de espuma o ciertos químicos que no son visibles. Estos problemas podrían provocar lesiones graves y requerir intervención médica para evitar lesiones permanentes”, se lee en el sitio web de la FDA. "El problema de la espuma PE-PUR puede resultar de la exposición a condiciones de calor y humedad y puede verse exacerbado por el uso de limpiadores de ozono u otros métodos de limpieza no recomendados por el fabricante".
La FDA tiene grabado 116,000 informes de dispositivos médicos y 561 muertes asociadas con dispositivos seleccionados desde abril de 2021. De las muertes reportadas, 187 se registraron entre el 1 de enero de 2023 y el 30 de septiembre.
Philips Respironics ha acordado con la FDA los términos de un decreto de consentimiento. La empresa ya no venderá CPAP, BiPAP ni dispositivos respiratorios en Estados Unidos, según un comunicado de prensa. Sin embargo, la empresa seguirá brindando servicio a los dispositivos que ya están en posesión de los proveedores de atención médica y proporcionará nuevos dispositivos, servicios, piezas de repuesto y accesorios fuera de los Estados Unidos.
Janet Gray, residente de White Settlement que sufre de apnea del sueño, les dijo a CBS News Texas que ella era una de las muchas que tenía uno de los dispositivos retirados del mercado y había recibido un dispositivo reacondicionado 18 meses después del retiro. Sin embargo, dijo que cuando lo recibió ya no tenía fe en la empresa y empezó a temer por su vida.
"Tienes miedo de irte a dormir porque si te vas a dormir sin él, podrías morir, pero si te vas a dormir con él, podría matarte en el futuro", dijo Gray en una entrevista de 2023, según CBS. “Así que simplemente duermo con él (el dispositivo C-PAP) y rezo”.
Desde entonces, Philips Respironics ha emitido un comunicado afirmando que los dispositivos y las muertes supuestamente asociadas no están relacionadas. Un correo electrónico a el expreso de dallas También explicó que alrededor del 93% de los MDR presentados desde abril de 2021 hasta diciembre del año pasado fueron “presuntos mal funcionamiento” que no implicaron lesiones o muerte.
Según las investigaciones realizadas hasta la fecha, Philips Respironics no ha encontrado datos concluyentes que vinculen estos dispositivos y las muertes reportadas en estos informes de dispositivos médicos. Es importante destacar que la presentación de un MDR en sí no es evidencia de que el dispositivo causó o contribuyó al resultado o evento adverso”, dijo un portavoz de la compañía, en la declaración proporcionada a el expreso de dallas. "Philips Respironics investiga todas las quejas y acusaciones recibidas sobre mal funcionamiento, lesiones graves o muerte".
Desde entonces, Philips Respironics ha reparado el 99% de los dispositivos de terapia del sueño afectados en todo el mundo. Estudios recientes también han confirmado que los dispositivos PAP afectados no aumentaron los riesgos de cáncer y que no se espera que la espuma PE-PUR cause "daño apreciable" a los pacientes, aunque se están realizando pruebas.
“La seguridad y la calidad del paciente siguen siendo la máxima prioridad de Philips en toda la empresa. Resolver las consecuencias del retiro del mercado de Respironics para nuestros pacientes y clientes es un área de enfoque clave y reconozco y me disculpo por la angustia y preocupación causada”, dijo Roy Jakobs, director ejecutivo de Royal Philips en el comunicado de prensa. "Estamos totalmente comprometidos a cumplir con el decreto de consentimiento, que es un paso importante y proporciona un camino claro a seguir".
En septiembre de 2023, Philips Respironics acordó pagar al menos 479 millones de dólares para compensar a los usuarios de estos dispositivos en un acuerdo de demanda colectiva. Los consumidores que sean elegibles para recibir el pago pueden presentar su reclamo en el sitio web del administrador del acuerdo.